國衛院發現抑制KDM4C可調節糖解作用 抑制癌細胞轉移
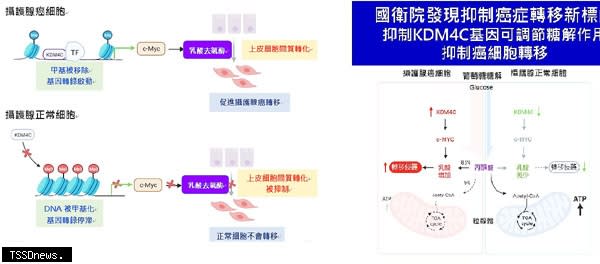
▲國衛院發現抑制癌症轉移新標的,抑制KDM4C可調節糖解作用抑制癌細胞轉移。
國衛院細胞及系統醫學研究所副研究員褚志斌研究團隊利用攝護腺癌細胞進行研究,發現剔除KDM4C後的癌細胞,與醣類、蛋白質與脂肪代謝的重要基因與蛋白質都有被抑制的現象,細胞內粒線體能量代謝跟有氧呼吸功能都出現失能,而讓癌細胞賴以為生的糖解作用訊號與產生ATP能量代謝的路徑,也受到抑制,證明KDM4C基因對癌細胞代謝扮演關鍵角色。抑制KDM4C可調節糖解作用,抑制癌細胞轉移。
癌症轉移可說是癌症治療最棘手之問題,同時也是癌症患者之主要死因,而酸化的環境有利於癌症轉移。癌細胞為了快速分裂,常利用步驟較少產能效率較低的無氧糖解快速產生能量,而非步驟較複雜但產生能量較多的有氧糖解,這種特殊代謝現象稱為瓦氏效應(Warburg effect)。癌細胞可利用無氧糖解之代謝產物作為細胞增生分裂的原料,代謝產生的乳酸還會酸化腫瘤環境幫助癌細胞轉移,因此如何抑制癌細胞的無氧糖解作用,成了癌症醫療的關鍵問題之一。
研究團隊透過一系列生化實驗證明KDM4C可以直接調控致癌基因c-Myc基因跟蛋白質的表現量,c-Myc是最著名致癌基因之一,不但調控癌細胞的生長、存活,還調控許多新陳代謝酵素,其中在細胞無氧糖解時,幫助細胞將醣類代謝物最後轉化為乳酸的乳酸去氫酶LDHA就是直接受到c-Myc所調控的,研究團隊證實,剔除KDM4C的攝護腺癌細胞,在醣解作用的代謝基因與代謝物皆受到嚴重影響,且不論是剔除KDM4C基因或是c-Myc基因,皆可以減少細胞分泌的乳酸,同時導致細胞內丙酮酸的堆積,降低了癌細胞的轉移能力。
目前已有學者著手開發KDM4C的抑制藥物,期望透過精準抑制腫瘤中的KDM4C/c-Myc/LDHA/糖解代謝,達到阻絕或延緩攝護腺癌轉移的新治療方針。

 Yahoo奇摩新聞
Yahoo奇摩新聞 
