早衰症治療新思維!陽明大學、國衛院研究成果登國際封面
科技部12日發布新聞稿表示,在科技部長期補助下,國立陽明大學與國家衛生研究院團隊合作研究發現罕見疾病「早衰症」重要的致病因素,成果更榮登歐洲分子生物學組織雜誌(EMBO Reports),並獲選為10月5日當期的封面。EMBO為國際知名生命科學領域組織,此一成果除受到國際重視外,也是將臺灣基礎科研實力推向國際的最佳典範。

科技部長期深耕基礎研究,支持國內研究人員進行各項科學研究,補助優質團隊追求學術卓越,在生命科學領域探究生命奧秘、找尋疾病機轉,進而創造科技突破造福人群。此次由國立陽明大學生化暨分子生物研究所講座教授陳鴻震研究團隊,與國家衛生研究院生技與藥物研究所副研究員紀雅惠合作發現,細胞初級纖毛(primary cilium)的異常可能是導致罕見疾病「早衰症」重要的致病機轉,這個發現提供一個開發早衰症治療策略的新思維。

早衰症Hutchinson-Gilford progeria syndrome (HGPS)患者在嬰兒時期就開始出現發育不良、皮下脂肪變少、產生皺紋、禿頭、骨質疏鬆、心血管疾病及關節出現問題等,平均壽命只有13歲。這個疾病最早是在1886年被發現,直到2003年才知道是因LMNA基因突變所致,但是病理機轉至今仍不清楚。LMNA基因表現A型核纖層蛋白(lamin A),是構成核纖層(nuclear lamina)的主要成分之一,扮演著細胞核骨架的功能,當LMNA基因發生突變,細胞核會出現不正常的皺摺現象,甚至凹陷變形。
除了早衰症之外,LMNA基因突變也與其他至少10種人類疾病有關,例如 Emery-Dreifuss肌肉萎縮症(muscular dystrophy)、擴張型心肌病變(dilated cardiomyopathy)等,這些疾病統稱為核纖層蛋白病症(laminopathy)。
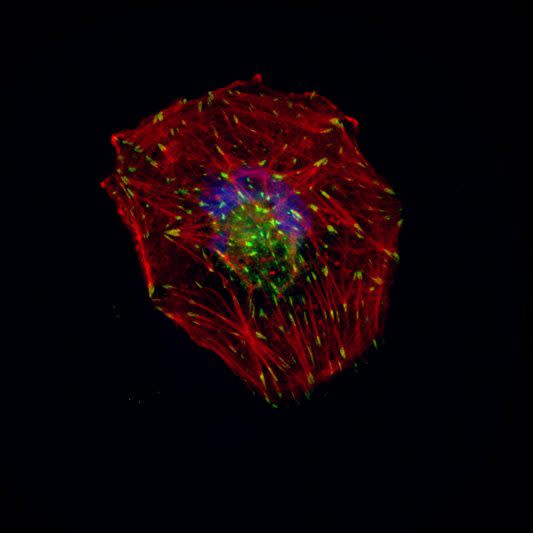
陳鴻震的研究團隊首先在早衰症病患的皮膚纖維母細胞中觀察到有較少及較短的初級纖毛,由於初級纖毛的功能就像是細胞的天線一樣,用於偵測細胞外環境的變化,進而傳遞訊息讓細胞可以調適。因此,推測初級纖毛的異常可能是導致早衰症重要的致病機轉。研究團隊進一步利用LMNA基因的缺陷小鼠進行實驗,證實在核纖層蛋白缺陷的早衰小鼠,許多器官的細胞初級纖毛都出現問題。接著團隊利用RNA干擾技術,在人類視網膜色素上皮細胞中降低核纖層蛋白的表現,也同樣造成初級纖毛的異常。
在機轉的研究方面,研究團隊發現LMNA基因的缺陷,會造成細胞微絲骨架(actin cytoskeleton)的過度組裝,進而干擾初級纖毛的形成。反之,若抑制微絲骨架的組裝則可恢復初級纖毛的形成。這項發現不僅有助於了解早衰症及其他核纖層蛋白病症(laminopathy)的致病機轉,也開啟了開發治療相關疾病的嶄新研究方向。

此次研究由科技部經費支持,由陳鴻震實驗室博士後研究員范嘉榕(第一作者) 主要負責執行;國衛院副研究員紀雅惠提供早衰症病患的皮膚纖維母細胞及早衰小鼠;陽明大學生化暨分子生物研究所教授游麗如及副教授王琬菁協助早衰小鼠的組織切片及初級纖毛的螢光染色及觀察。陳鴻震以優質的研發能量,集合各領域專家合作,將臺灣研究成果推向國際;更以優異的統籌規劃能力,自去年借調至科技部生科司擔任司長,未來將以領頭羊的角色繼續帶領臺灣生命科學領域朝國際頂尖學術目標邁進。

 Yahoo奇摩新聞
Yahoo奇摩新聞 