國產疫苗來了!高端二期解盲成功聲明
記者簡浩正/台北報導
我國疫情嚴峻,疫苗成為民眾抗疫期待。高端疫苗今10日暫停交易,下午5點舉行重大訊息記者會,公布新冠肺炎二期臨床期中的解盲成果,外界預期應可核准通過,將向疾管署申請(Emergency Use Authorization, EUA)緊急授權藥證許可,預期7月可提供國人開打。
記者會上,高端總經理陳燦堅宣布,高端新冠疫苗二期臨床試驗解盲成功,在安全性上,所有受試者未出現不良反應。拚7月上市,提供國人開打。
高端疫苗副總李思賢說明,高端二期今年1月22日開始進行第一位受試者疫苗施打,並於4月28日完成所有受試者第二劑疫苗接種。根據藥物主管機關的技術性要求與試驗設計,此臨床試驗已於5月28日達到所有受試者第二劑疫苗施打後一個月、以及中位數受試者追蹤二個月的期間分析條件。
他說,受試者血清依據主管機關要求,以中研院P3試驗室完成中和效價,在盲性狀態下,上傳至第三方臨床試驗受託機構,今年6月10日下午一點召開獨立科學委員組成的獨立監測委員會(IDMC)進行進行解盲。內容為以下幾點:
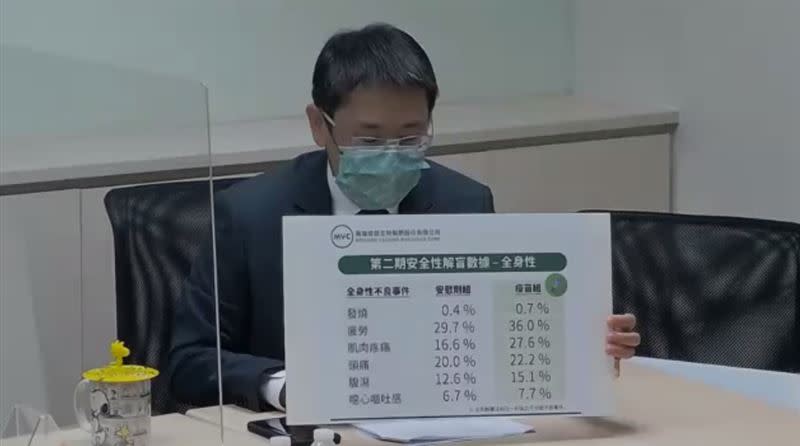
一、安全與耐受性良好,受試者沒有嚴重不良反應。
二、免疫生成部分,不區分年齡組情況下,疫苗組在施打第二劑後28天的血清陽轉率達99.8%
三、本公司將盡快將期間分析報告,儘速送食藥署進行EUA審查授權。
【後續開發計畫】
1. 本公司將盡速將二期臨床主試驗期間分析數據、以及研發相關文件,送交至食藥署,申請EUA緊急授權使用審查。
2. 依據二期期間分析數據,本公司將盡快向歐盟EMA及其他藥證主管機關諮詢及申請第三期臨床試驗,以取得疫苗常規藥證以及國際認證為目標。
3. 本項新冠疫苗二期臨床主試驗持續進行中,根據試驗計畫書,受試者將繼續完成6個月追蹤。
4. 除了本項二期主試驗,本公司目前仍同步有多項臨床評估進行中,都將依規劃持續進行。包含:以第一期受試者追加第三劑疫苗施打的延伸性試驗,測試第三劑追加劑的安全性與免疫原性。高齡族群的高劑量比較試驗,測試安全性與免疫原性。擴大年齡層,評估12~18歲青少年族群的臨床試驗。

據了解,新冠肺炎疫苗將是高端疫苗第一個上市產品,也將成為台灣第一個成功上市開打的本土疫苗公司,指標意義重大。高端也於昨9日晚發布重訊表示,今股票交易暫停。不過,面對政府在此前就簽下500萬劑預購合約、高端股價狂飆、中研院院士陳培哲閃辭等疑點,仍有諸多疑慮,也有擔心解盲失敗的聲音。
指揮中心指揮官陳時中,今下午也在疫情記者會上針對高端疫苗解盲表示,解盲是科學數據出來與相關研究,綜合資料才會送到審查委員會審查,才做施打可能性。不過現在都還無法做任何預測。
更多三立新聞網報導
6診所「與柯P關係好」才拿到疫苗?阿中:請北市府提報告
三重診所醫因「隱形缺氧」死?莊副:7天前曾接種AZ疫苗
小禾馨4診所拿85瓶AZ 蘇怡寧:打院內醫護且依法造冊
快訊/好心肝打千人疫苗遭嚴辦!晚間記者會突取消改發聲明

 Yahoo奇摩新聞
Yahoo奇摩新聞 