高端執行歐盟EMA疫苗免疫橋接第3期試驗 爭取歐盟認證
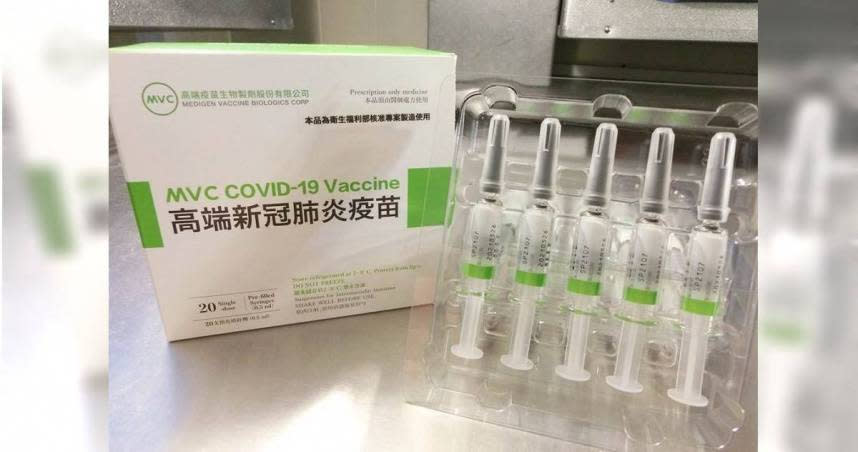
[周刊王CTWANT] 美國宣布11月起,外國成年旅客入境須完整接種兩劑疫苗才可入境,據世界衛生組織現階段共核准7種疫苗,除了美國核准的莫德納、BNT及嬌生外,還有AZ、中國國藥、中國科興及Covishield(印度版AZ),至於我國產高端疫苗是否有機會獲得國際認證?高端疫苗於22日公告,高端新冠肺炎疫苗在歐盟之第3期試驗,將規劃以多國多中心方式,與歐盟已上市之新冠肺炎疫苗進行免疫橋接比對試驗,目標盡快取得歐盟認證。
高端表示,今年6月由全球主要國家之法規單位所組成的「ICMRA國際藥物監管機構聯盟」,已於會議中達成以免疫橋接進行臨床試驗設計的目標共識。在ICMRA會議之後,日本藥政法規單位PMDA已核准日本第一三共藥廠,以免疫橋接方式執行3期試驗;韓國藥政法規單位MFDS,也在ICMRA會議後,核准韓國SK藥廠,以3990人規模,與AZ比較進行3期免疫橋接試驗。
另外,在日韓核准國內藥廠以免疫橋接執行新冠疫苗3期臨床試驗之前,法國疫苗廠Valneva,今年4月21日於英國取得3期IND許可,並在6月3日完成招募4000名受試者,預期年底將可取得全病毒去活化新冠疫苗VLA2001與AZ疫苗的免疫橋接3期期中分析數據。
高端表示,除了日韓以外,由澳洲、加拿大、新加坡、瑞士、英國所組成的「AccessConsortium跨國醫藥聯盟」,也在今年9月16日發表聯合聲明,表態支持ICMRA的會議結論,將以免疫橋接方式授權新的新冠肺炎疫苗。
這次取得歐盟EMA正面回應後,高端董事會通過新冠肺炎歐盟3期免疫橋接試驗初步預算,並確認相關試驗設計原則,後續會依歐盟EMA之科學諮詢結論建議,盡快向EMA提出3期臨床試驗申請,包括巴拉圭的臨床試驗也持續進行中,將用於取得當地臨床資料以進入中南美洲市場。
看更多 CTWANT 文章
入秋首波東北風週五到!颱風「電母」週六前生成 最新路徑曝光
遭前公司求償怒批:過河拆橋!文姿云合約訴訟結果出爐 獲判35萬
瘋狂男粉絲假扮外送員 闖女直播主閨房性侵6次「勒索近9千元」

 Yahoo奇摩新聞
Yahoo奇摩新聞 